云舟生物科技(广州)股份有限公司品牌商
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
载体家课堂 | 一文了解高特异性神经示踪工具--重组狂犬病毒
547 人阅读发布时间:2023-09-27 13:47
神经示踪是神经解剖学和脑功能研究的常用实验手段。神经示踪技术从最早期的银染法、放射性示踪剂、再到荧光染料和病毒示踪工具,已经过数十年发展,在特异性、灵敏性、分辨率等维度上不断提升。病毒示踪工具的一大优势是病毒具备自我复制的能力,因此可产生较强的神经示踪能力。除了表达荧光报告基因,病毒载体还可以导入其它受细胞时空可控表达的转基因,从而开发出特异性更强的神经环路示踪工具。这些作为神经示踪工具的病毒载体可分为顺行和逆行;跨突触和非跨突触等类型。其中狂犬病毒(Rabies virus, RV或RABV)的一些特定毒株仅能在连接神经元间进行逆行跨突触传播,且毒性较低不影响神经元细胞代谢,是一种优秀的嗜神经病毒载体。
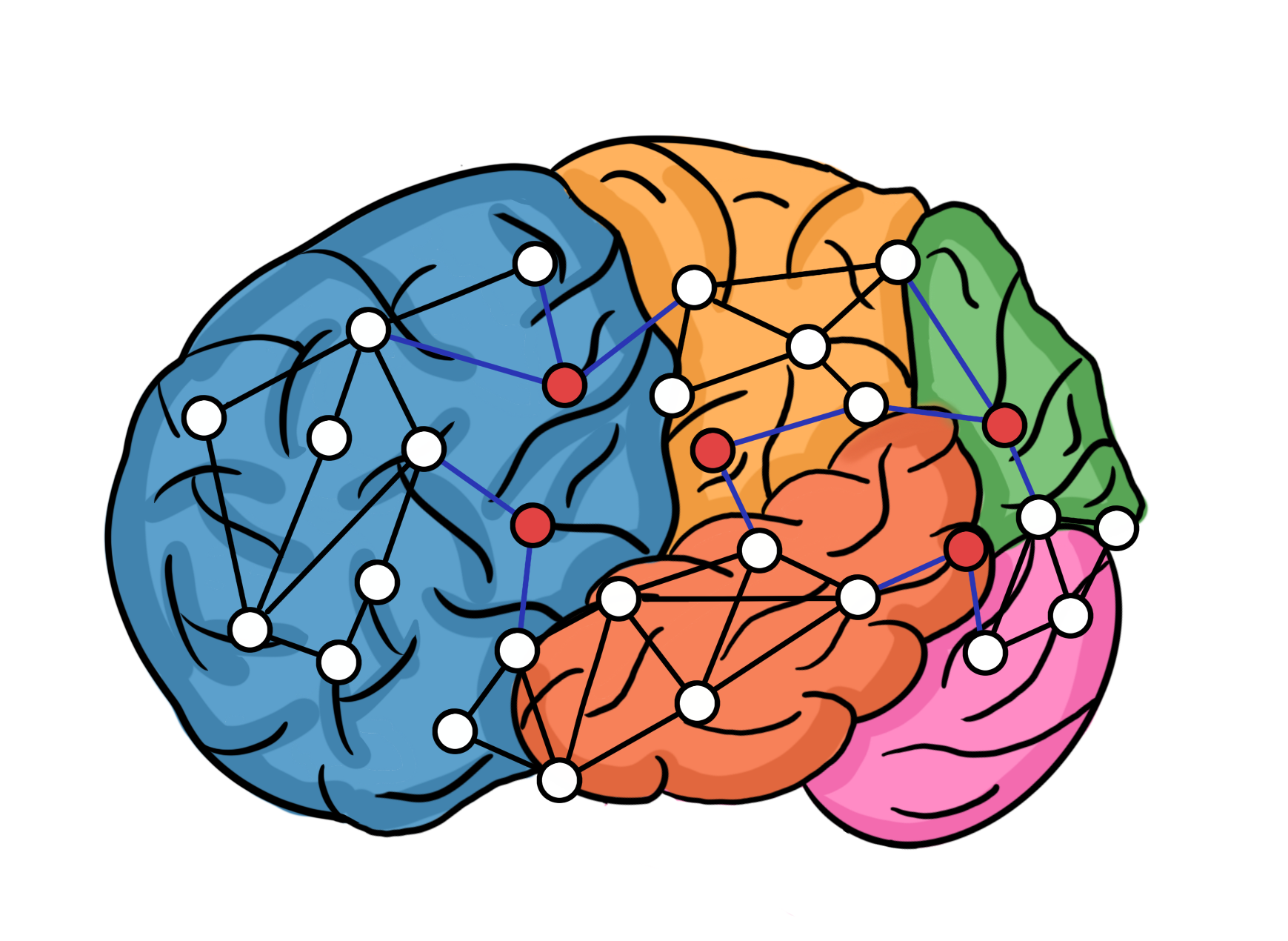
大脑神经示踪图示
狂犬病毒(RABV)
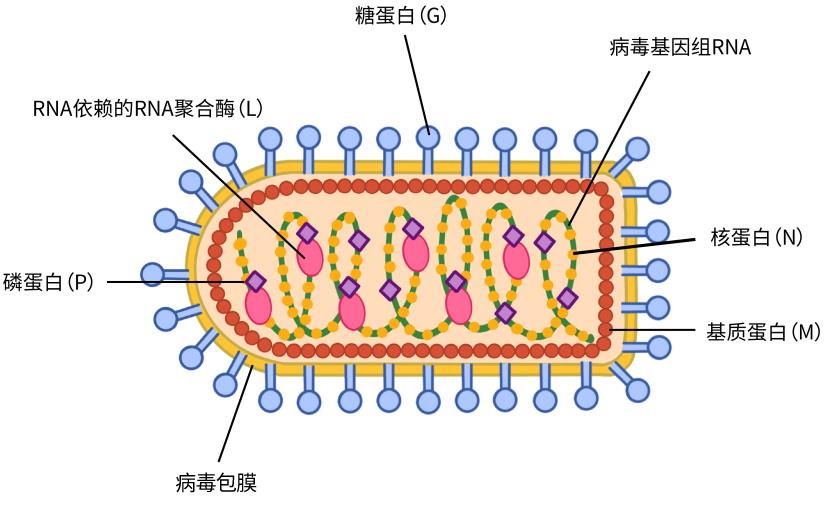
RABV的病毒结构示意图
RABV在结构上与VSV病毒相近,同属于弹装病毒科。RABV的基因组为长度12 kb的单股负链RNA,编码5种蛋白,即核蛋白(N)、基质蛋白(M)、RNA 依赖的 RNA 聚合酶(L)、磷蛋白(P)和糖蛋白(G)。与VSV不同的是,RABV的G糖蛋白被证明与神经元轴突末端的受体特异性结合,由此提供了RABV神经嗜性。一旦进入轴突末端,病毒就会逆行传输到细胞体并进行复制。RABV的病毒复制和转录均发生在细胞质中,最大限度地减少了整合宿主基因组的风险,同时降低了病毒生命周期对宿主机制的依赖。
RABV作为神经示踪工具应用时,通常需要删除RABV病毒自身的G糖蛋白基因以限制病毒的出芽和传播;另一方面,通过置换原始的G糖蛋白产生RABV假病毒,可以使其跨突触感染神经元的能力受实验操控。经过重组改造的RABV病毒载体,可装载约3-5 kb的目的基因,同时在其病毒包膜上可使用不同的糖蛋白类型以满足不同的实验需要。
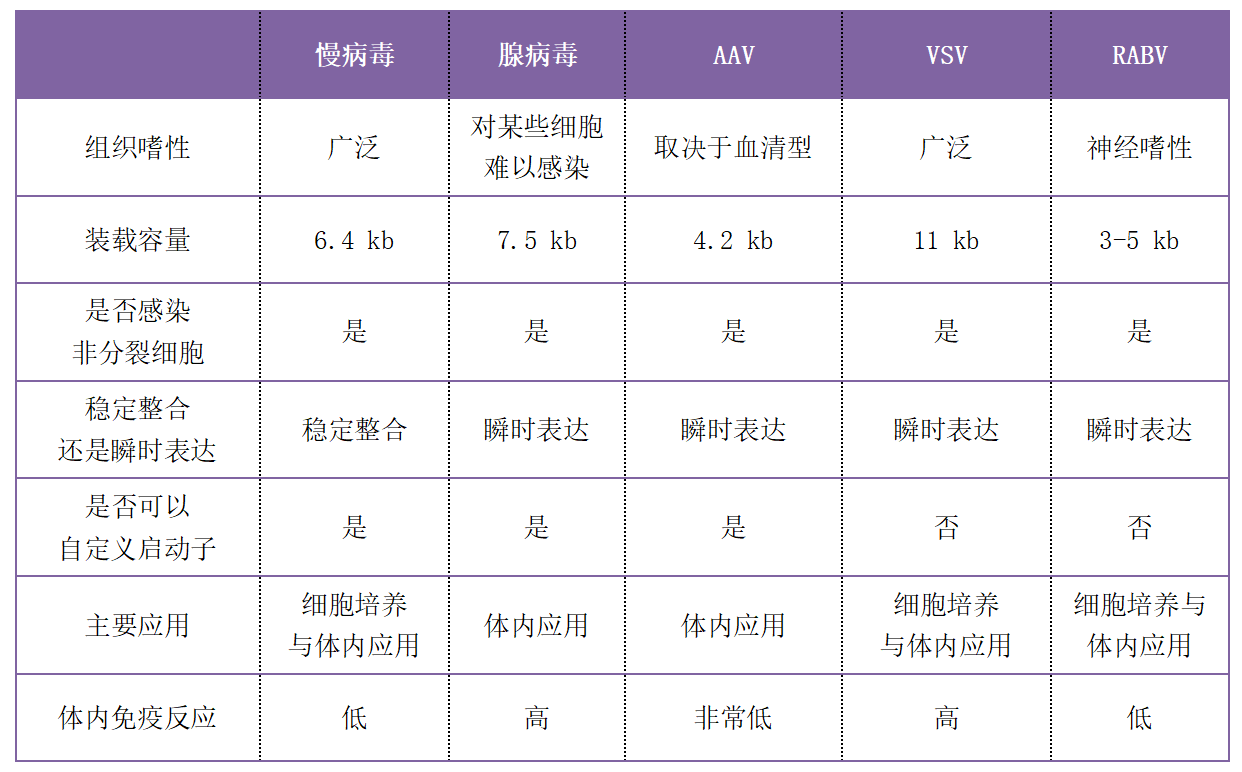
RABV与多种其它病毒载体比较
第一代神经示踪RABV是从RABV疫苗株SAD-B19删除G糖蛋白基因获得的SAD-B19(ΔG)。该种毒株的病毒颗粒具有良好的热力学稳定性,在生产上可得到较高的滴度,在神经元中也能表达较高水平的标记基因。然而SAD-B19(ΔG)存在着跨突触传递能力低、具有长期神经毒性等不足。为改进这些问题,Reardon等人(2016年)建立了CVS-N2c(ΔG)突变株,表现出相比SAD-B19更强的逆行跨单突触传递能力和更低的毒性的优势。G糖蛋白假型化的CVS-N2c(ΔG)毒株可实现逆行标记投射网络,但是未能用于特定神经元中的单突触连接研究。RABV神经示踪的进一步发展为此增强了其单突触限制性——这有赖于TVA/EnvA系统的开发使用。
TVA是一种禽类特有的细胞表面受体,哺乳动物神经系统中无内源性表达。EnvA则是重组的禽类肉瘤病毒(Avian sarcoma leukosis virus,ASLV)的包膜蛋白,可特异性识别结合TVA。在TVA/EnvA系统中,首先使用表达TVA和G糖蛋白的AAV辅助病毒感染第一级神经元,此时再转导EnvA假型化的RABV。RABV-EnvA仅能特异性感染表达TVA的第一级神经元,然后复制生成可感染第二级神经元的G糖蛋白假型化的病毒颗粒。由于第二级神经元中缺乏G糖蛋白补偿,进入该胞体的RABV中仅能完成RNA复制,但不产生成熟的病毒颗粒继续跨突触感染。因此,TVA/EnvA系统广泛被应用于逆行单突触跨一级神经元标记。
重组狂犬病毒免费申请试用活动
云舟生物在CVS-N2c株基础上开发了多种G糖蛋白基因突变的RABV重组病毒,可使用G糖蛋白(N2cG或B19G)或EnvA糖蛋白假型化。我们对RABV-EnvA进行了体外转导验证,证明其有效转导表达TVA受体的细胞。

表达EGFP的RABV转导293T细胞(表达或无表达TVA)。转导后48小时使用荧光显微镜成像。放大倍数:100×。左:明场。右:EGFP。
活动详情请点击:重组狂犬病毒免费申请试用活动-云舟生物 (vectorbuilder.cn)