云舟生物科技(广州)股份有限公司品牌商
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
基因疗法从科研走向临床应用的关键——如何对载体进行优化?
723 人阅读发布时间:2024-10-31 09:30
对于基因疗法开发,一个优秀的基因递送载体设计需要完成从科研阶段到临床前研究的无缝过渡。对比科研载体设计,临床应用所需的载体需要考虑更多关键因素,如细胞和基因治疗药产品的效用、安全性和可制造性等。为保证基因疗法药物的最终效果,优化载体设计是一个必要且需要仔细考察多因素的过程。
载体效用考量
对于每一个载体元件,其序列都必须经过深入的设计和实验测试以使其发挥良好的作用。首先,启动子序列可显著影响基因表达水平。通过仔细调整这一区域的序列可以有效提高载体的效用。此外,通过优化治疗性基因的编码序列,也可以促进基因被正确翻译,增加其有效表达。
对于细胞和基因疗法开发,其它需要采取的策略性优化措施还包括优化GC含量和CpG岛,还需要应对隐性剪接位点和过早的polyA信号等挑战性问题,并确保mRNA/IDR三级结构经过优化达到很低的水平。
除了载体序列本身外,载体组件的位置排列对于顺利地实现载体功能以及最大限度地减少非必要的序列相互作用。此外,还需要选择适当的载体系统,优化包膜蛋白或衣壳以靶向特定组织,进行高效的基因递送,进一步促进临床试验的成功。
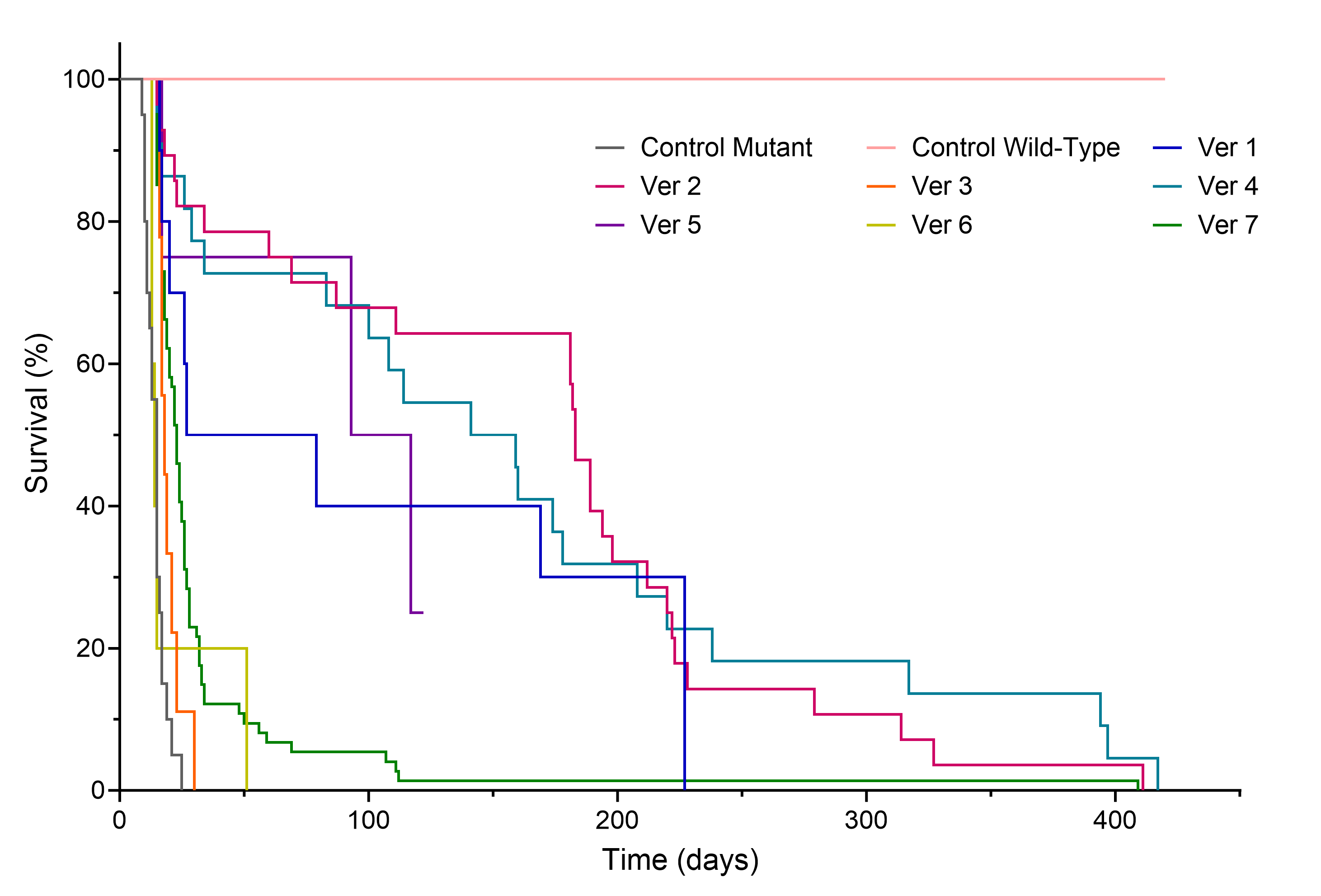
云舟生物比较了使用不同的启动子序列驱动表达的治疗性基因药效。图中展示了接受重组AAV9基因替代疗法的小鼠生存率。实验还同时观察了野生型对照和未接受治疗的突变型小鼠。
安全性考量
安全性对于细胞和基因治疗载体的在临床环境中的成功应用至关重要。药物开发人员必须考虑各种涉及安全性的因素,包括抗生素选择、含有病毒来源的调控元件以及载体成分的毒性和免疫原性。在临床前载体中选择抗生素筛选标记是一个特别重要的决策,因为许多常用的抗生素不符合临床法规。因此,建议从临床前阶段开始使用卡那霉素。此外,相比于ORF,常用的WPRE调控元件也具有安全性问题。对此可选择WPRE3或突变型WPRE这样的替代序列。
可制造性考量
基因治疗载体的可制造性涉及多种因素,包括需要确保上游和下游过程的可扩展性、产量和质量的可重现性以及法律合规性。通过考量载体骨架、宿主菌和发酵条件,可提高载体生产的质量和产量。通过优化临床前载体的特定产量和体积产量,可分别带来更高质量的DNA和更具成本效益的载体生产。
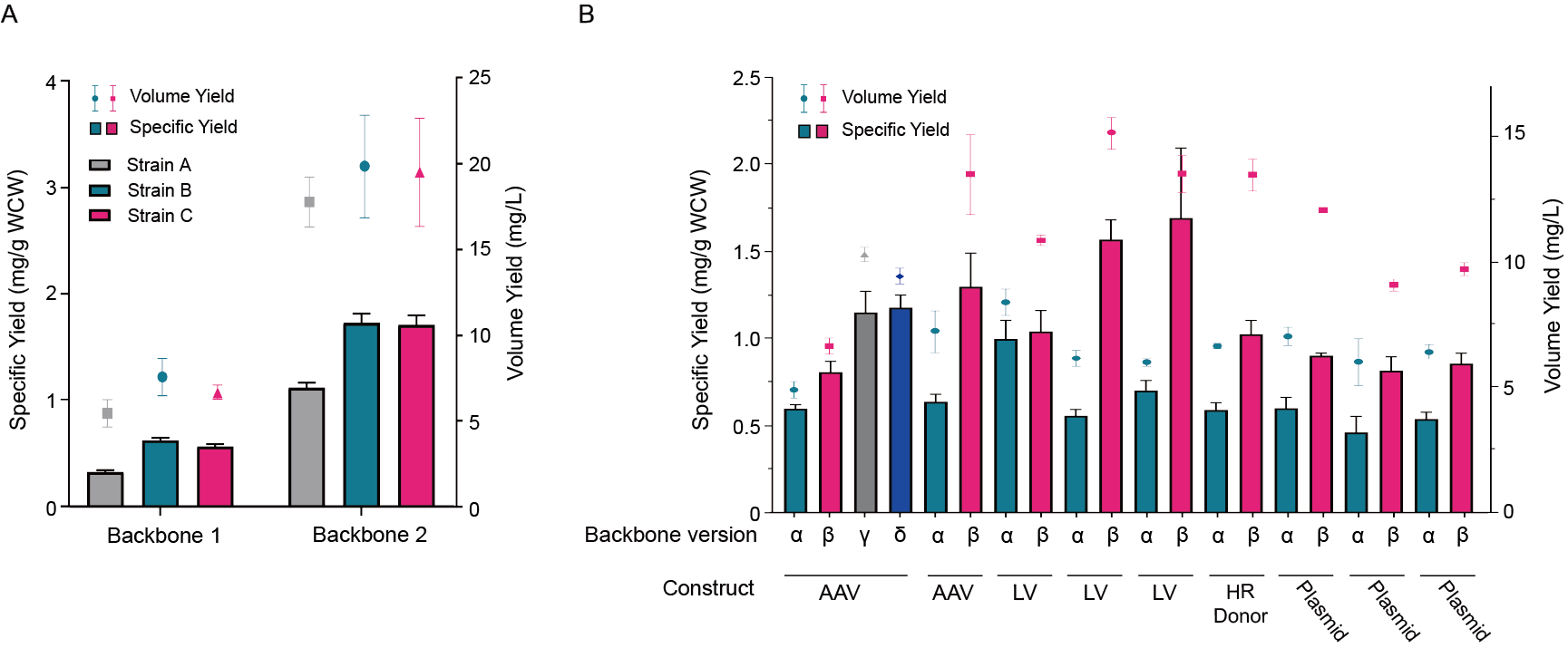
云舟生物通过宿主菌优化和骨架优化提升载体产量。载体克隆使用了不同的骨架,在实验室规模下进行发酵测定特定产量(柱)和体积产量(点)。
序列筛选
云舟生物的cliniVec™设计团队与体内体外筛选服务专家密切合作,可为您筛选应用于基因治疗的各种载体序列。我们提供多种类型的筛选项目,除了载体衣壳序列筛选,还包括启动子和编码序列筛选等。我们提供从文库构建到NGS测序和验证的端到端筛选服务。与我们的cliniVec™设计团队合作,获得为您量身定制的高精度且可靠的序列筛选解决方案,提高载体开发的成功率。
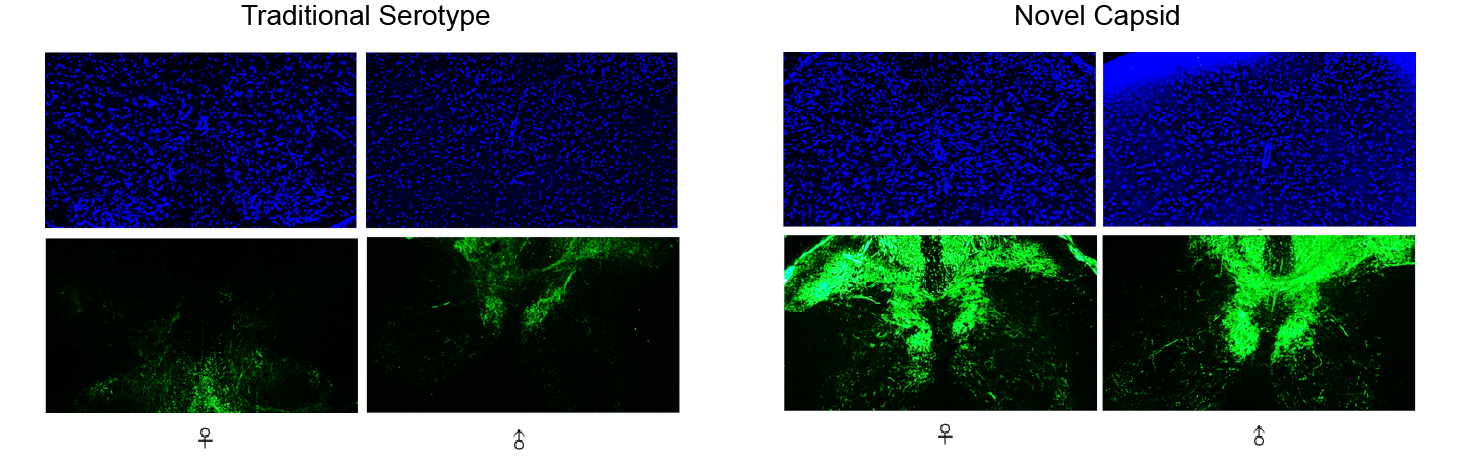
云舟生物采用衣壳进化筛选方法后的新型AAV衣壳。AAV转导小鼠颈椎,对比衣壳优化前的传统血清型AAV与优化后的新型衣壳AAV的转基因(CMV>EGFP)递送效率。
cliniVecTM载体优化项目