云舟生物科技(广州)股份有限公司品牌商
8 年
手机商铺
- NaN
- 0
- 1
- 0
- 3
公司新闻/正文
科研干货 | 多基因递送载体如何设计?
2647 人阅读发布时间:2024-03-01 10:30
基因递送载体不仅只递送单个目的基因,而是通常连携多个组件,如启动子、开放阅读框(ORF)和标记基因等一同递送。这些载体经过定制,可以设计出包含多个ORF、多个与之融合或连接的报告基因,甚至包括整个表达盒。高效递送这些组分需要考虑多种因素,特别是在使用慢病毒载体的时候。
为此,我们总结了以下要点以帮助您构建一个表达高效的多基因表达载体。
不同的基因以不同的启动子驱动表达
对于使用具有大容量载体如piggyBac,单载体上表达多个基因的一种方法是插入多个独立的表达盒。这种方法的优势在于可以使用不同的启动子和表达系统,而且由于为每个目的基因插入了一个独立的启动子、开放阅读框和polyA尾巴,可以确保独立转录事件的发生。
但需要注意的是,大多数载体系统都可能被设计成包含多个表达盒,尤其是慢病毒载体。慢病毒中的长末端重复序列(LTR)不仅在整合基因组序列中起作用,其还是病毒重组基因组的转录起始和终止位点。慢病毒载体的3' LTR自身就会提供polyA加尾信号,而在慢病毒载体表达盒中引入额外的polyA将过早地终止转录。此时由于3' LTR未被转录,病毒滴度将降低。
翻译的重启和跳过机制
对于慢病毒和常见的载体系统,引入多个ORF的常见选择是创建多顺反子设计——多个基因放置在单个启动子下游,并在其之间放置连接子(Linker)。此时所有ORF一起被转录为单个mRNA链,连接子的存在则促使每个ORF被独立翻译为单个多肽。最常用的连接子是IRES和2A肽(P2A、T2A、E2A和F2A)。下表比较了这两类连接子的特点。

考虑到这些连接子的不同特性,当使用超过两个ORF时,或当需要近似的ORF表达水平时,我们建议选择2A肽。当表达超过两个ORF时,应使用不同的连接子(如P2A和T2A)以避免重组。在2A肽家族中,我们推荐P2A,因为其切割效率最高,或T2A,其效率略低。当第二个ORF的低表达水平不影响实验结果时,例如当第二个ORF是药物筛选标记时,建议可使用IRES。
ORF放置顺序
在决定插入多个ORF的连接方式后,下一步需要考虑的要点是ORF的放置顺序。在优化多顺反子表达时,ORF的相对位置对表达的影响是一个不可忽视的因素。已有多项使用荧光蛋白的研究表明,每个基因的表达水平取决于其在多顺反子转录物中的位置。为了在更接近生理相关的背景下研究不同排列对基因表达的影响,我们比较了三个内源性基因。这些基因使用六个多顺反子慢病毒载体,每个载体放置3个基因组合排列的方式进行表达。我们使用P2A和T2A作为第一和第二个连接子(图1A)。
比较不同位置中特定基因的表达水平(图1B和1C),当ORF最接近启动子时,通常会观察到最高的表达水平。当ORF位于第三个位置时,观察到最低的表达水平——第一个位置相比至少降低了80%。
有趣的是,单个基因的相对表达水平不仅受其自身位置的影响,还受其其它两个基因的顺序的影响(图1B)。例如,当Gene B位于第一个位置(载体3和载体4)时,其表达水平最高;然而,当Gene C位于第二个位置时,Gene B的表达与Gene A相比增加了5倍(载体3对比载体4)。在这两种载体中,第二个基因的表达水平受到了极大的影响。
虽然ORF的表达水平通常在移动到离启动子的远端位置时会急剧下降,但其它ORF在多顺反子载体中的排列也会影响表达水平。通过优化目的基因的位置,可以在实验中实现特定的表达目标。
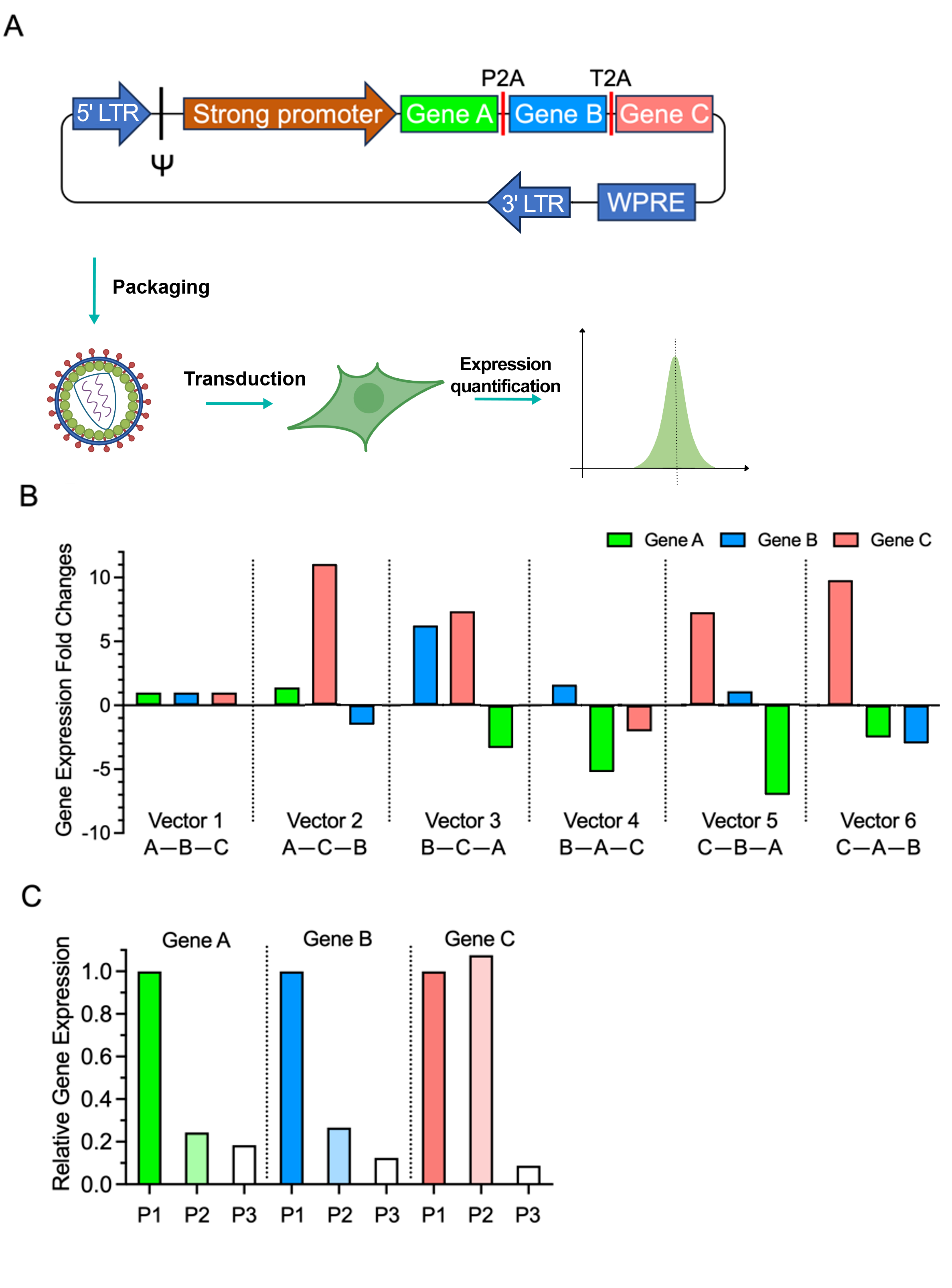
图1. 2A连接的多顺反子载体中位置依赖性基因表达水平的比较。(A)携带三个ORF且中间以P2A、T2A间隔的三个慢病毒载体被包装成慢病毒。哺乳动物细胞随后被转导,并通过流式细胞术评估三个ORF的所有六种排列模式中每个基因的表达。(B)这六种排列包括A-B-C、A-C-B、B-C-A、B-A-C、C-B-A和C-A-B。为了便于更直接的比较,我们将每个基因在任何给定排列中的表达水平与A-B-C顺序中的表达水平进行齐一化。(C)比较三顺反子载体中特定位置的蛋白表达水平。我们将不同位置的每个基因的表达水平齐一化为其在第一个位置的表达水平。
总而言之,由于细胞类型、载体递送系统、所需启动子数量以及不同基因的具体表达要求,在靶细胞中表达多个基因具有多种可实现的方法。在使用慢病毒载体时,则因为3’ LTR自身的polyA加尾信号性质,多基因共表达存在明显的限制。通过仔细考察连接子和目的基因的顺序,则可有进一步优化表达水平。对于多基因共表达载体云舟生物拥有丰富的设计经验,如果您有任何疑问欢迎与我们联系。
参考文献
[1] Guntaka RV. Transcription termination and polyadenylation in retroviruses. Microbiol Rev. 1993 Sep;57(3):511-21.
[2] Hager S, Frame FM, Collins AT, Burns JE, Maitland NJ. An internal polyadenylation signal substantially increases expression levels of lentivirus-delivered transgenes but has the potential to reduce viral titer in a promoter-dependent manner. Hum Gene Ther. 2008 Aug;19(8):840-50.
[3] Liu Z, Chen O, Wall JBJ, Zheng M, Zhou Y, Wang L, Vaseghi HR, Qian L, Liu J. Systematic comparison of 2A peptides for cloning multi-genes in a polycistronic vector. Sci Rep. 2017 May 19;7(1):2193.
[4] Shaimardanova AA, Kitaeva KV, Abdrakhmanova II, Chernov VM, Rutland CS, Rizvanov AA, Chulpanova DS, Solovyeva VV. Production and Application of Multicistronic Constructs for Various Human Disease Therapies. Pharmaceutics. 2019 Nov 6;11(11):580.