云舟生物科技(广州)股份有限公司品牌商
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
一文带你了解云舟生物自研创新前沿技术——助力高效基因递送
4 人阅读发布时间:2026-05-11 10:13
在细胞与基因治疗(CGT)领域,功效、安全性和可制造性被视为决定基因递送技术转化的三大基石。VectorBuilder针对基因递送过程中的技术瓶颈进行深耕,旨在开发更具效率且经济实惠的解决方案,以降低药物研发风险,提升治疗效果与效率,改善安全性指标,并使产品具备临床和商业化应用的条件。
新型AAV衣壳
在众多的基因递送系统中,腺相关病毒(AAV)因其低致病性和良好的基因转导能力而应用广泛。基于AAV的基因疗法往往受限于转导效率低下和递送脱靶的问题,因此不得不提高给药剂量来弥补性能不足,进而提升了成本和毒性风险。VectorBuilder的创新衣壳技术提供了一种有效解决方案:经过工程化改造的衣壳具有更高的靶向特异性和更好基因递送性能,可实现安全的、更有效且更高效率的基于AAV的治疗方案。
当前,VectorBuilder推出工程化改造的多种新型AAV衣壳:包括可有效穿透血脑屏障的、可穿透视网膜且高效转导视网膜色素上皮细胞(RPE)的、以及高效靶向肌肉组织等应用类型的专用衣壳。这些衣壳已在特定动物模型中得到验证,具有优异的靶向性且极低的脱靶表达。
专有递送系统
当前次世代疗法的应用潜力仍受传统基因递送方法的束缚。这类方法存在诸多局限,包括有效载荷量有限、易引发不良免疫反应、放大生产工艺复杂等。而对于AAV递送系统而言,还额外面临载体稳定性不足的问题。我们凭借前沿技术打造的先进基因递送系统克服了以上的挑战性问题。
MiniVec™质粒
VectorBuilder所采用的专有MiniVec™质粒采用了微型化骨架结构,支持无抗生素、无培养基添加剂的克隆筛选方式,并且可被应用于多种类型的表达系统,可实现更高的有效产量和翻译效率。经我们测试在疫苗递送模型中,注射MiniVec™质粒可以成功激活急性和长期免疫应答。值得一提的是,所有体内实验均未表现出任何机体或生理层面的不良反应。
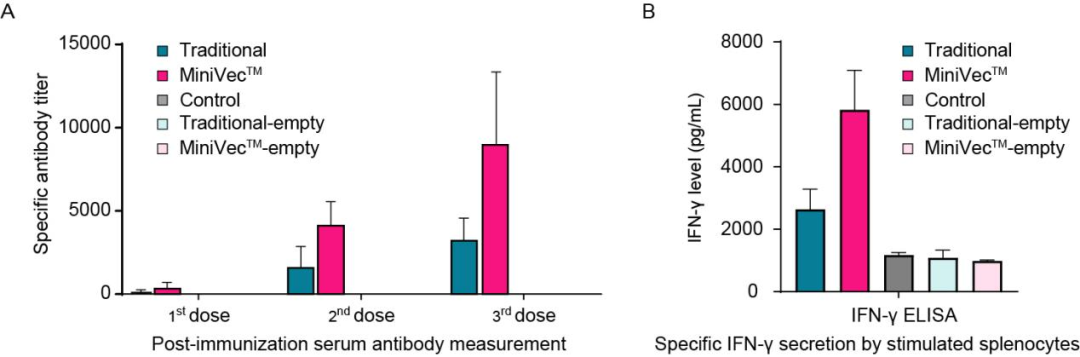
图1 使用裸DNA免疫法对比传统质粒与MiniVec™质粒在表达COVID-19刺突蛋白时所诱导的免疫应答。分别向BALB/c小鼠肌肉注射三次,每次间隔两周的等摩尔量传统疫苗或MiniVec™疫苗、阴性对照(PBS)以及溶剂对照(传统空质粒或MiniVec™空质粒)。(A)在每次接种的两周后,下次免疫前,对动物采血检测特异性抗体效价。实验第42天,采集脾细胞。脾细胞培养物上清液用于检测由刺突蛋白免疫激活的(B)总IFN-γ分泌水平。
MuteFree™ AAV骨架
ITR序列是AAV包装与转基因表达过程中发挥关键作用的功能序列。然而,该区域GC含量高,稳定性极差且极易发生突变,而这类突变将降低包装效率和病毒滴度,转基因的表达效率也会受到影响。
针对这一问题,VectorBuilder开发了可保障ITR稳定性的新型AAV转移载体——MuteFree™ AAV。经过优化的载体骨架可帮助您的病毒载体彻底规避ITR突变问题,助力您精准把控基因治疗产品的特性、功效与安全性。该载体由我们的创新研发团队精心优化与验证,可为基因治疗产品提供符合要求的质量一致性保障。
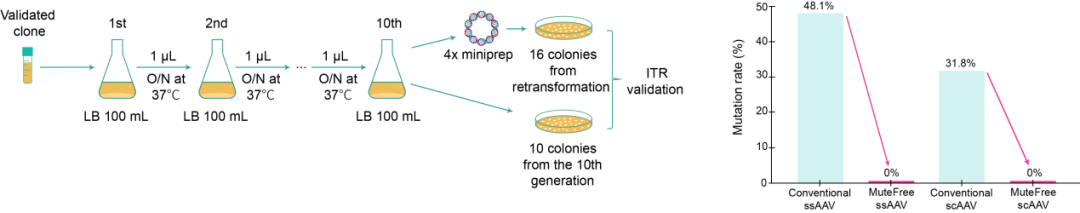
图2 MuteFree™ AAV可显著增强ITR稳定性。常规AAV骨架、MuteFree™ ssAAV和scAAV骨架分别在 E. coli 中连续传代10次后,检测其ITR突变率。使用MuteFree™ AAV骨架构建后,ssAAV的ITR突变率从48.1%降至0%,scAAV的ITR突变率从31.8%降至0%。
MegaAAV™递送系统
传统AAV载体通常存在包装容量限制,仅能携带小型转基因,这为基因治疗方案的开发带来了极大阻碍。尽管现有双AAV系统可通过将超大基因拆分至多个载体克服容量限制,但受递送效率低、无法完整重组得到有功能的转基因的限制,该系统的临床应用潜力仍存在较多局限。借助创新的体内重组策略,我们的专有多AAV递送系统可显著提升所递送基因的转录水平。该平台设计灵活,在超越双载体递送形式的同时还可递送更大的基因片段或实现复杂的多元件系统表达。
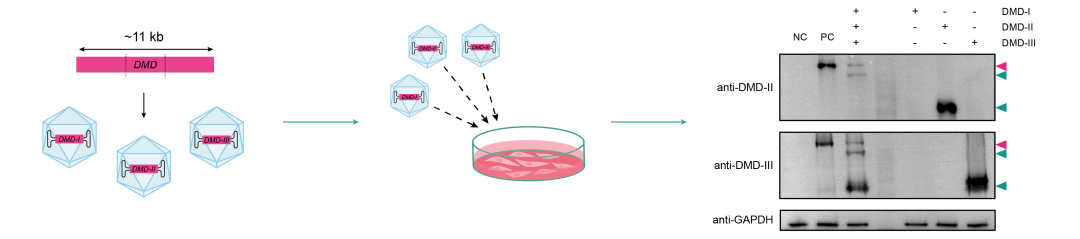
图3 使用MegaAAV™分割载体系统在体外成功实现DMD的功能重建。将人DMD 基因(约11 kb)分割为三个部分(DMD-I、DMD-II、DMD-III),并分别包装到独立的AAV载体中。将包含3种AAV病毒的MegaAAV™和每种AAV病毒各自转导HEK293T细胞(MOI=10^5 per AAV),转导后48小时收获细胞裂解物。未转导细胞(NC)和转染含有全长DMD质粒的细胞(PC)作为对照。所有样本均使用针对DMD-II和DMD-III中的特异性区域的抗体进行Western blot分析。粉色箭头指示DMD基因的体外完全重建,青色箭头指示DMD片段。