云舟生物科技(广州)股份有限公司品牌商
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
Autophagy | 中山大学联合云舟生物开发基于自噬体靶向递送的广谱流感疫苗新策略
12 人阅读发布时间:2026-05-11 10:23
为何流感疫苗需要年年更新,却仍难以保持稳定的保护效果?根本原因在于病毒持续发生抗原漂移,而当前主流疫苗主要依赖针对血凝素(HA)的抗体应答,一旦靶点发生变异,保护效果便会迅速下降。
相比之下,流感病毒的另一表面抗原——神经氨酸酶(NEU)因结构更为保守,长期被视为理想的广谱疫苗靶点。然而,NEU天然免疫原性较低,难以有效激发强烈免疫反应,尤其难以有效激活T细胞免疫。而后者恰恰在应对病毒变异、提供交叉保护中至关重要,却长期未被传统疫苗策略充分利用。
近期,一项发表于Autophagy的研究提出了一种全新的解决思路:通过将NEU抗原定向递送至自噬途径,重塑其抗原呈递路径,从而显著增强T细胞免疫应答。
该研究由中山大学孙彩军、舒跃龙及陈耀庆团队与云舟生物团队合作完成。同时,云舟生物为研究提供了关键的重组VSVΔG载体支持。

研究结果表明,这一“自噬靶向”创新策略不仅显著提升了NEU特异性T细胞应答的强度与广度,还在多亚型流感病毒模型中实现了有效的交叉保护,为广谱流感疫苗研发提供了全新思路。
1、NEU融合抗原的构建与功能验证
为了探究如何通过自噬途径增强NEU的免疫原性以应对流感病毒异亚型感染,研究人员首先设计了NEU-LC3B融合抗原,评估其靶向自噬途径的可行性。
研究团队利用重叠PCR技术将全长NEU的C端与LC3B的N端融合,构建了重组DNA载体和缺失G基因的重组水疱性口炎病毒(VSVΔG)载体。Western blot实验在293T细胞中验证了目标蛋白的成功表达。
进一步的底物裂解及酶联凝集素测定法(ELLA)评估显示,NEU-LC3B融合蛋白保留了NEU的关键抗原表位,同时其降低的酶活性可能有助于提升作为疫苗抗原的安全边界。
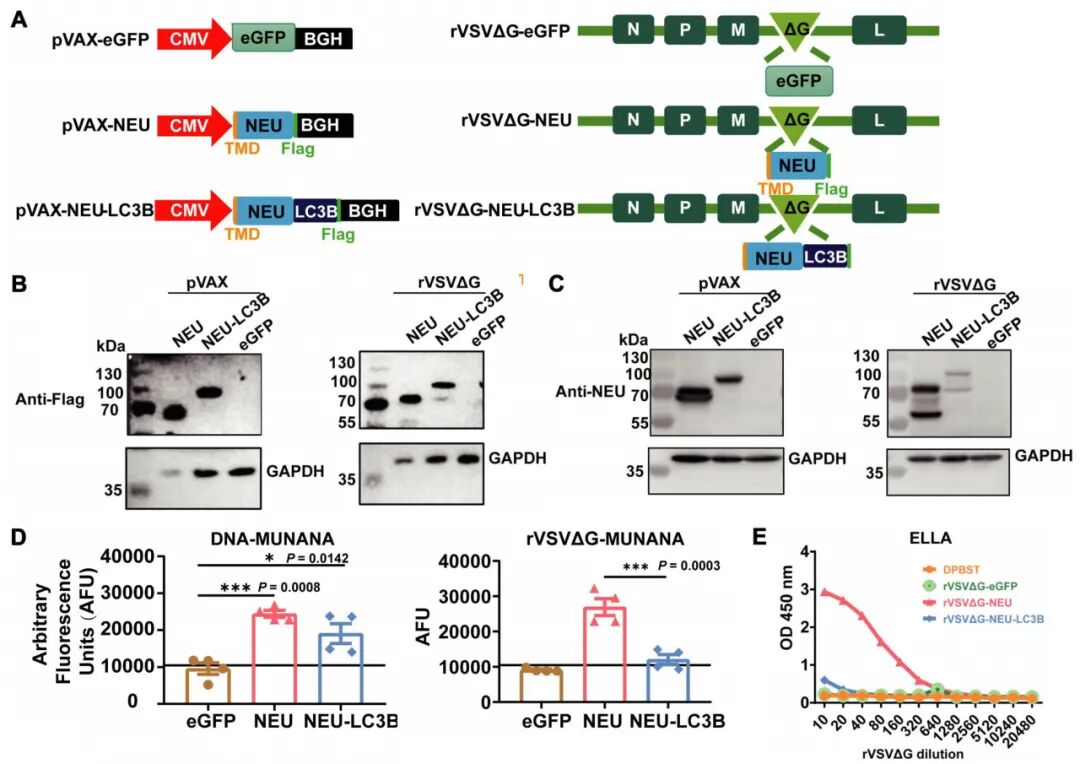
图1 NEU基础构建体的分子设计及表达验证
2、NEU抗原的自噬通路重定向
为了验证设计的NEU-LC3B融合蛋白是否能够精准激活自噬-抗原呈递通路,研究团队深入考察了该蛋白在细胞内的亚细胞定位情况。
在HeLa及DC2.4细胞中,共聚焦显微镜结果显示:单独表达的NEU呈弥散分布,而NEU-LC3B则形成明显点状结构,提示其参与特定细胞器过程。通过氯喹阻断溶酶体降解或雷帕霉素调节自噬通量后,NEU-LC3B与LC3B、溶酶体标志物LAMP2以及MHC II区室均表现出显著共定位。
这些发现共同表明,融合抗原NEU-LC3B能够被有效重定向至自噬体,并经由自噬-溶酶体途径降解,随后由MHC II区室进行高效递送。
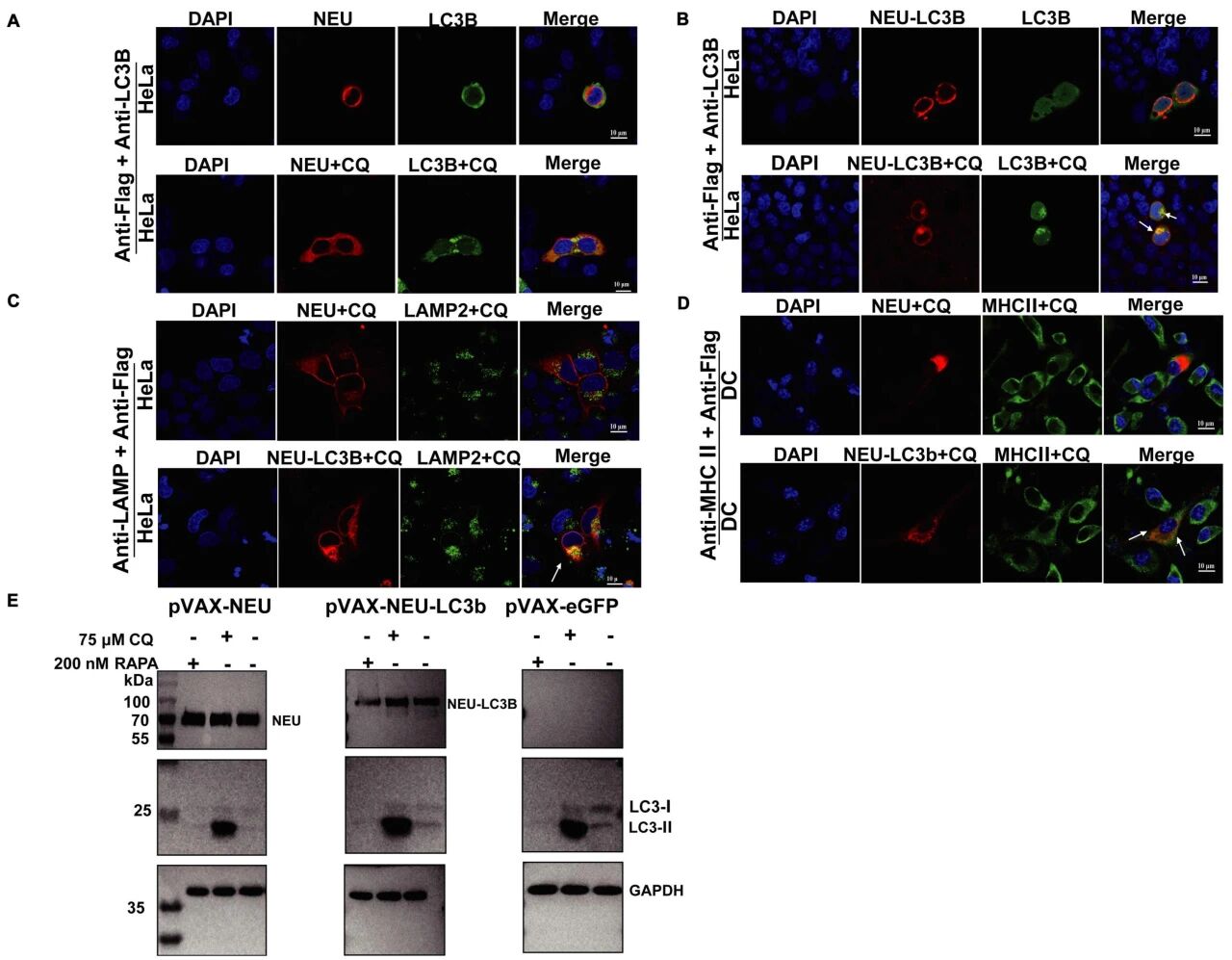
图2 融合蛋白在细胞内向自噬及抗原呈递相关区室的靶向定位
3、体内特异性免疫应答诱导
在确认了体外细胞层面的靶向性后,研究团队进一步在小鼠模型中评估了该融合抗原对细胞和体液免疫应答的实际激发效果。
采用DNA初免结合rVSVΔG加强免疫的方案,ELISA结果显示,NEU-LC3B可诱导以Th1型为主的抗体应答(IgG2a偏向),提示其免疫极化方向更有利于抗病毒反应。
在细胞免疫层面,IFN-γ ELISpot及胞内细胞因子染色结果显示,与NEU组相比,NEU-LC3B显著提高了分泌IFN-γ、TNF和IL-2的CD4+及CD8+ T细胞频率。同时,CD8+ T细胞的细胞毒性标志物CD107a表达也明显增强。
这些数据表明,NEU-LC3B策略成功诱导了更为强效的NEU特异性T细胞免疫,显著提升了T细胞的反应规模与多功能性。
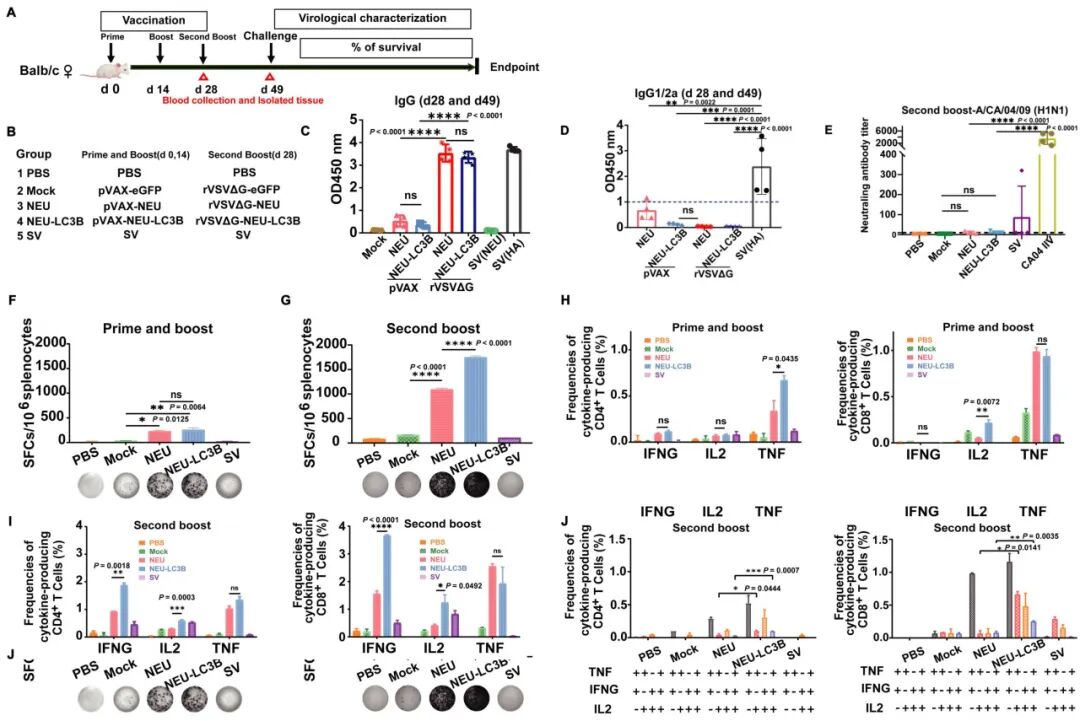
图3 NEU-LC3B构建体激发小鼠抗原特异性免疫反应的全面评估
4、T细胞免疫表位图谱解析
为从机制层面解析免疫增强的来源,研究团队对NEU特异性T细胞表位进行了系统性解析。
研究利用覆盖NEU全长的92个重叠多肽构建了20个肽池,通过ELISpot和ICS筛选,不仅证实了多肽42是NEU中最具优势的T细胞表位,还成功鉴定出一系列此前未见报道的全新NEU特异性T细胞表位。此外,研究还预测并比对了疫苗株与异亚型攻毒株间高度保守的CD8+ T细胞表位。
这表明NEU-LC3B免疫不仅能够诱导更强烈的CD4+和CD8+T细胞反应,还促使机体识别出多个全新的T细胞表位,大幅拓宽了免疫应答的广度。
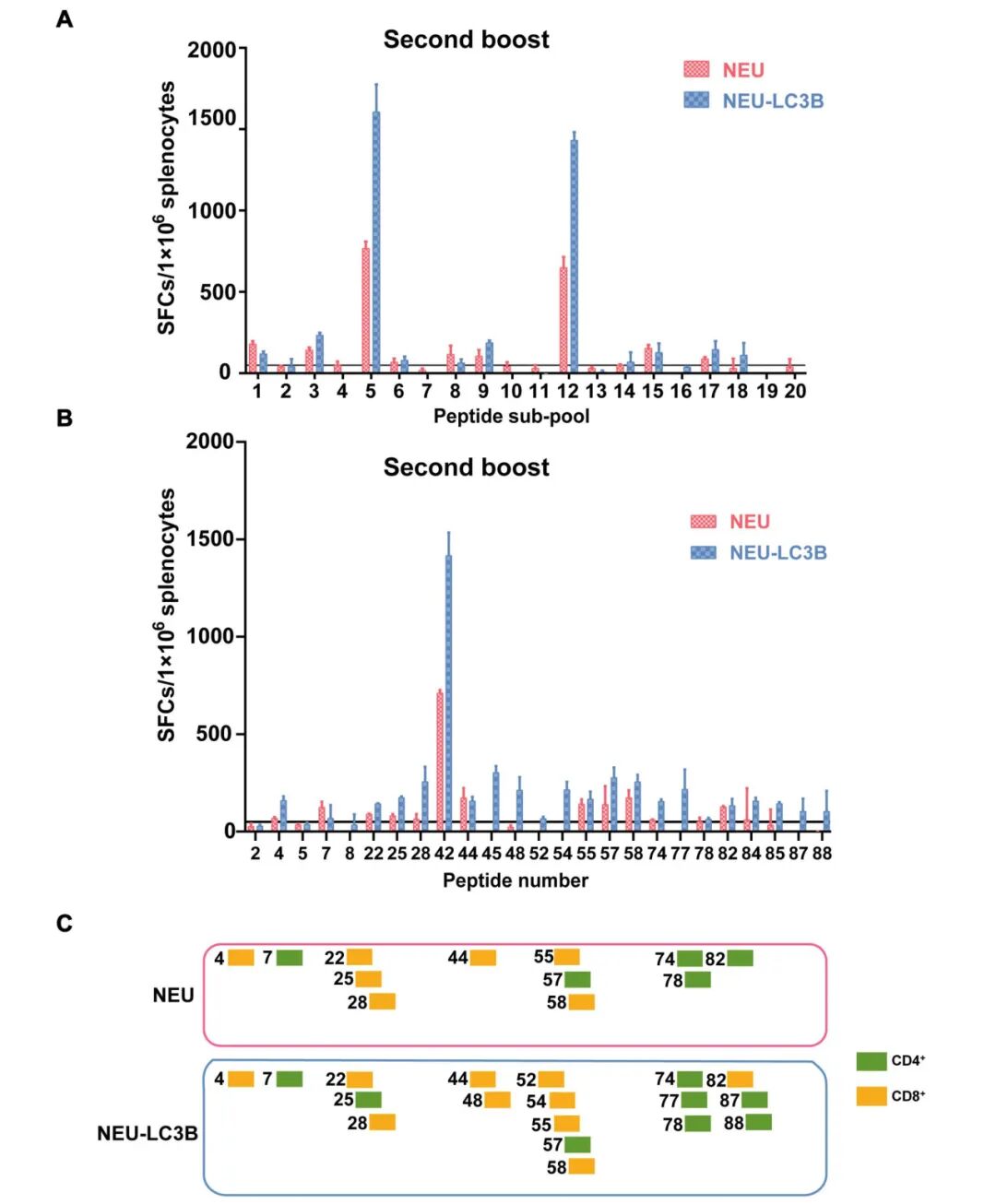
图4 基于NEU-LC3B免疫应答的新增CD4+与CD8+T细胞表位鉴定
5、多亚型流感病毒保护效力验证
为验证免疫增强是否能够转化为实际保护效果,研究在小鼠模型中开展了多种流感病毒攻毒实验。
在同源H1N1(A/CA/04/09)攻击下,NEU-LC3B免疫组小鼠体重稳定、全部存活,肺部病毒滴度迅速降至检测限以下,组织病理损伤亦显著减轻。在异源同亚型PR8(H1N1)模型中,该策略同样表现出良好的交叉保护。
更具意义的是,在抗原差异更大的异亚型H3N2(A/Aichi/2/1968)致死性攻击中,NEU-LC3B组仍实现约60%的存活率,而传统疫苗组则全部死亡。
结果确证,基于NEU-LC3B的疫苗构建体不仅能够对同源流感毒株提供彻底的保护,还对具有高度抗原差异的异亚型毒株展现出了卓越的交叉保护功效。
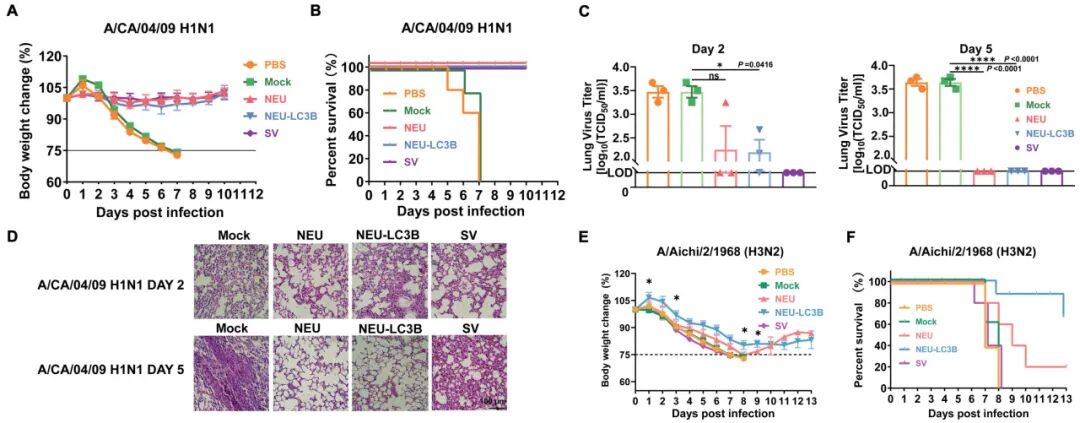
图5 疫苗策略对同源及异源流感病毒攻击的体内保护效果评估
6、T细胞是保护效力的核心驱动力
为明确免疫保护的效应机制,研究进一步通过体内T细胞耗竭实验进行验证。
在免疫小鼠中分别清除CD4+和CD8+ T细胞后再次进行H1N1攻击。结果显示:依赖抗体免疫的传统裂解疫苗组仍保持100%存活;而NEU-LC3B组的保护效力则显著丧失,小鼠死亡率明显上升,且幸存个体表现出严重体重下降。
该耗竭实验直观地证明了,由本研究策略所诱导的NEU特异性T细胞免疫在抵抗流感病毒感染、提供存活保护中发挥了不可或缺的关键作用。
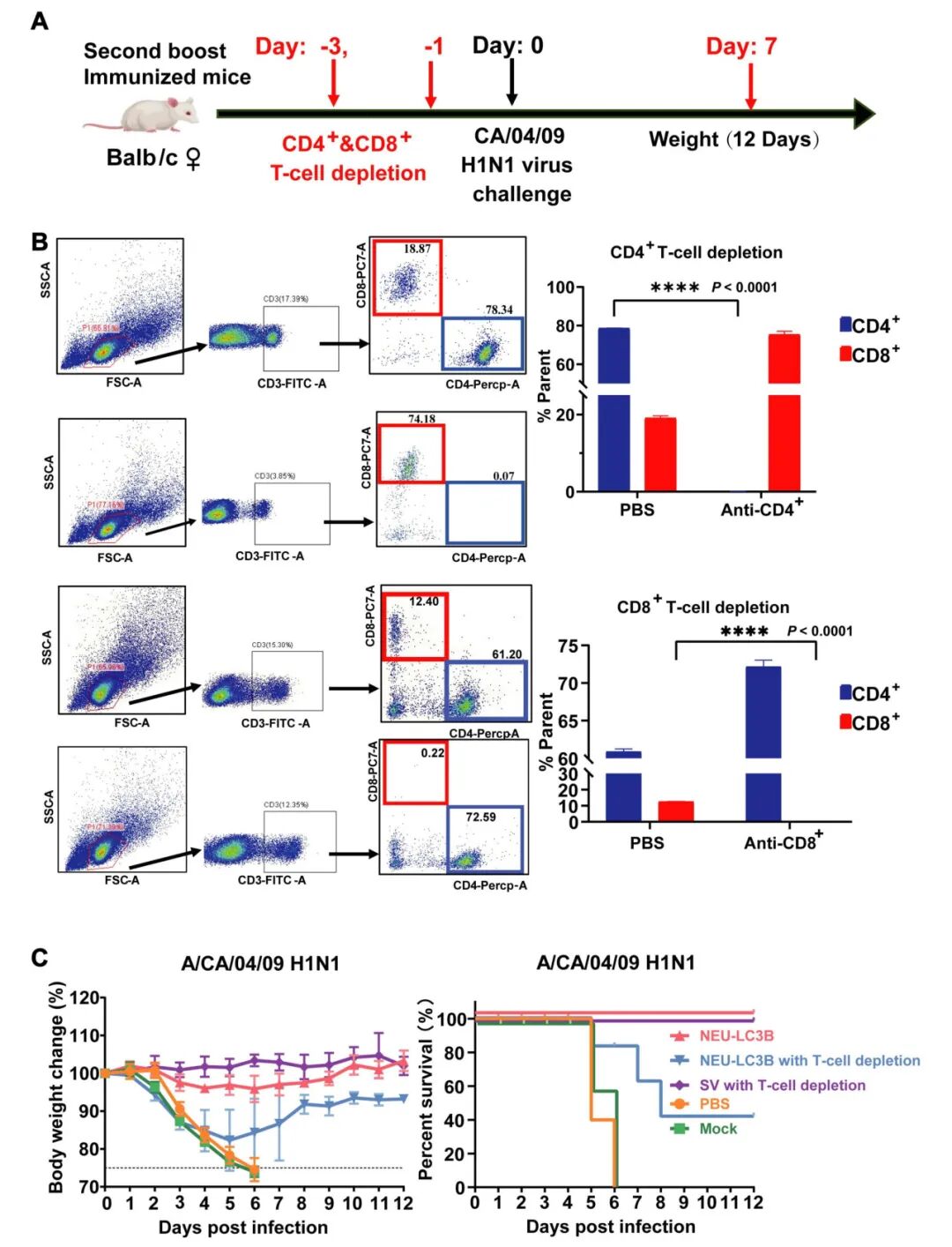
图6 特异性T细胞免疫介导疫苗保护效力的机制验证