云舟生物科技(广州)股份有限公司品牌商
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
一文了解质粒DNA、RNA、RNP非病毒系统递送CRISPR组分的不同特点
1810 人阅读发布时间:2025-03-06 11:29
CRISPR/Cas9基因编辑如今已对生物学研究带来了革命性的影响,通过对基因的敲除、敲入、转录激活或抑制,这种技术已在包括从研究细胞和动物模型中的基因功能到修改农作物的基因修饰,再到开发编辑人类的致病基因的基因疗法等领域有所广泛应用。
CRISPR基因编辑的相关组分可以通过多种方式包括病毒的和非病毒的形式递送至靶细胞。这些递送方式均有其各自的优缺点,本文将对比多种非病毒基因递送系统特点,并提供其应用在不同类型实验中的关键要点。
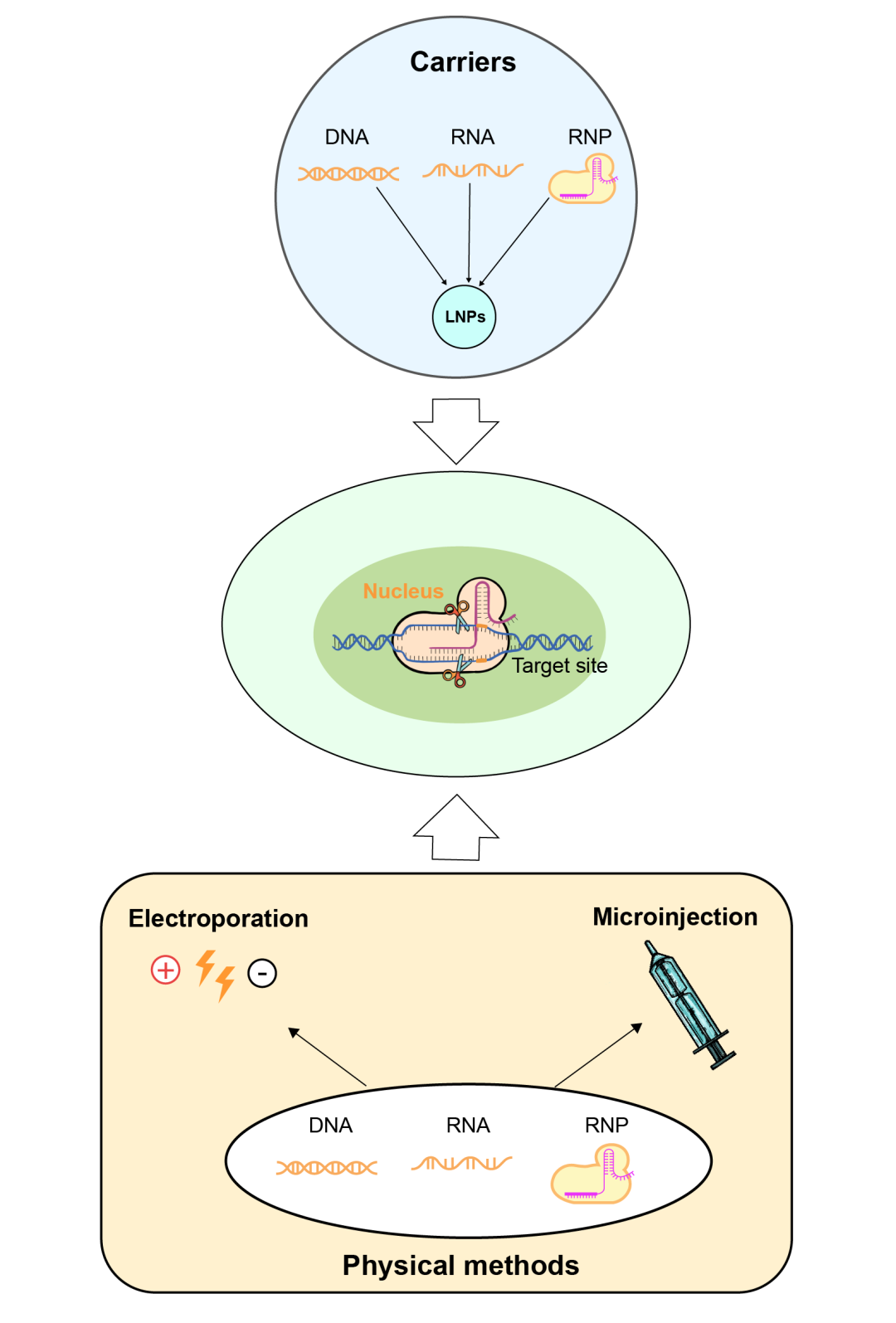
图1 非病毒方式递送CRISPR组分
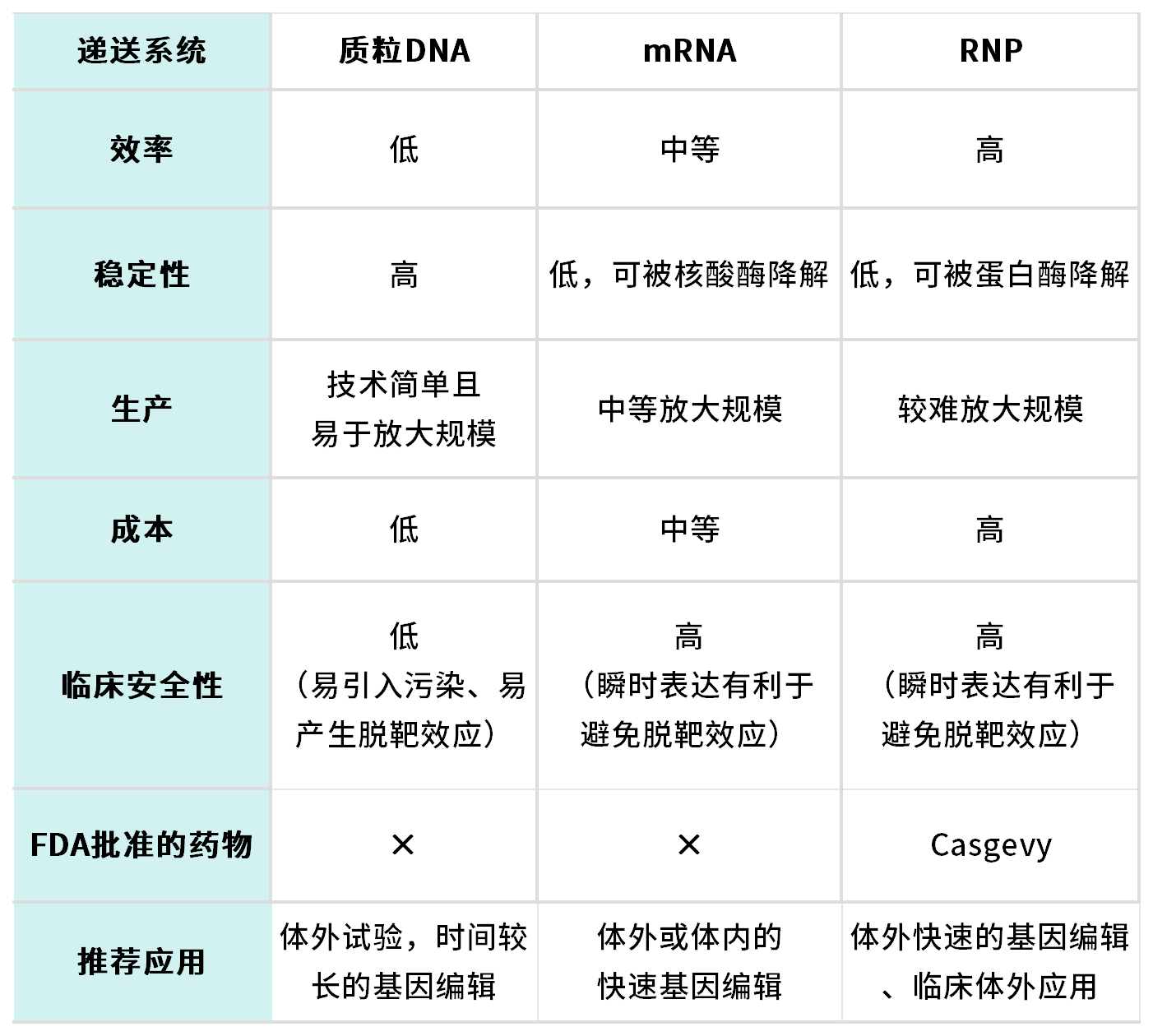
质粒DNA递送系统
引入外源遗传物质最简单且最低成本的方法是直接转染质粒DNA(pDNA)。一个质粒载体可以同时携带Cas9核酸酶和gRNA的编码序列,也以使用两个质粒载体各自携带这两种组分。质粒递送的特点是基于DNA固有的稳定性,可以实现较长时间且稳定的转基因表达。特别是对于靶点位于DNA被高度压缩的高级染色质结构的情况,一个较慢的且持久的CRISPR组分表达过程更有利于确保CRISPR基因编辑机器随时间增加而到达这些靶位点。但是一个相伴随的风险是,持续的Cas9表达也会导致非靶位点的切割风险增加,造成更显著的脱靶效应。此外,质粒DNA也具有整合到宿主基因组中而引起插入突变的风险。
为减少脱靶效应,利用质粒递送系统应考虑在Cas9上引入额外的修饰,比如偶联一个降解信号序列或者活性抑制结构域,又或者使用诱导表达系统表达CRISPR组分。常用的诱导表达系统可以使用四环素响应元件(TRE)启动子驱动表达Cas9。当体系中存在四环素或其类似物(例如多西环素)时,该系统会被激活。如果需要在同一种细胞类型中进行多次编辑实验,建议使用带有四环素诱导Cas9表达的细胞稳转株进行实验,以最小化背景编辑并实现长期和大规模的基因编辑效果。
质粒的生产相对简单且易于放大规模,但是在质粒制备过程中存在内毒素污染的风险,而且一些为细菌扩增而设计的序列可能会引发不必要的宿主免疫反应。为克服质粒的安全性问题,可以考虑使用微环质粒DNA骨架(比如miniVec®)。这类质粒骨架中删除了大部分与细菌序列有关的元件。
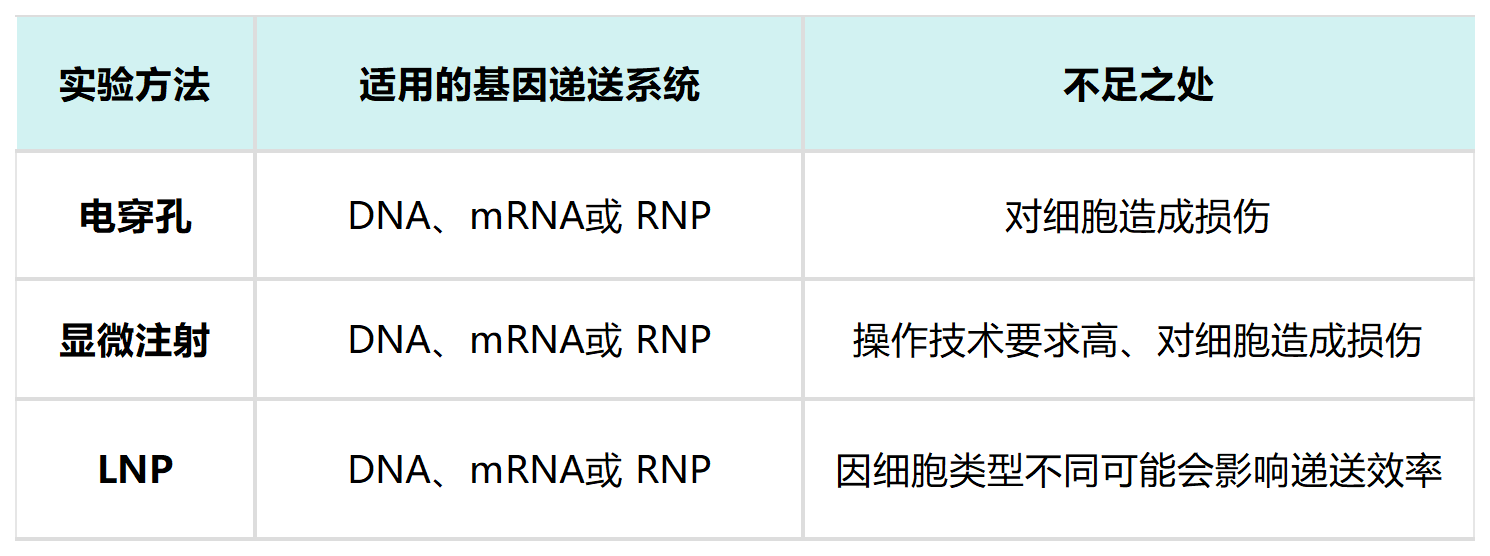
与病毒递送系统不同,非病毒的CRISPR递送方法需要额外的组分来帮助穿过细胞膜。对于质粒,可以采用物理方法(如电穿孔和显微注射)或封装系统(如脂质纳米颗粒(LNP))。其中,LNP特别受到临床应用的青睐。与物理方法相比,LNP对靶细胞的损伤更小,为其装载物提供了一个保护性的胶囊结构,提高了递送组分的稳定性,延长其在血液内的循环时间。然而,相对于电穿孔和基于病毒的递送方式,LNP由于依赖于细胞的内吞途径,进入细胞的效率会更低。
考虑到DNA递送的复杂性以及使用质粒递送CRISPR组件会带来的脱靶效应风险,目前在开发的CRISPR基因疗法均没有使用这种递送系统。相反,由于质粒生产简单且成本效益高,它更适合用于基础研究,特别是靶细胞可被用于观察脱靶效应的情况。
RNA递送系统
将CRISPR组分以RNA(Cas9 mRNA和gRNA)的形式进行递送是一种比使用质粒更高效的方法,它绕过了转录过程,并立即在细胞质中启动Cas9的翻译。这种递送方式特别适合于短期实验,因为RNA的固有不稳定性导致其在宿主体内会被迅速降解,因此CRISPR组分的表达是短暂的。总体而言,这种特性防止了Cas9的长时间表达,有利于减少脱靶效应,并且被认为相比于可能带来插入突变的质粒DNA递送方式更为安全。由于mRNA可以在体外以无细胞方式生产,因此在生产过程中具有较低的污染风险。然而,RNA的制造过程比pDNA更为昂贵且技术更复杂,其大规模生产也更具挑战性。
与pDNA类似,mRNA可以通过显微注射、电穿孔或者LNP的方式送入细胞中。对于治疗性RNA,基于LNP的递送已被证明是一种有效的方法——辉瑞和莫德纳的COVID-19疫苗都采用了这一策略。未来使用mRNA LNP的CRISPR疗法的新突破将在针对治疗甲状腺素淀粉样变性(ATTR)的药物的1期临床试验中进一步体现。值得留意的是,这种疗法是在体内进行基因编辑的,对比目前获批的在体外进行基因编辑的疗法,其时间和人力上花费的成本更高。
核糖核蛋白复合体(RNP)递送系统
递送CRISPR组分效率最高的非病毒方法是使用核糖核蛋白复合体(RNP)。由于无需转录和翻译,Cas9蛋白和gRNA可以进入细胞核可以立即启动基因编辑。此外,与RNA一样,这种方法没有外源基因整合宿主基因组的风险,其CRISPR组分表达是短暂的,有利于最小化脱靶效应。然而,RNP易被蛋白酶降解,这使得其与质粒和mRNA相比稳定性较差,对使用和储存时的条件要求有所挑战,特别是在临床环境中。此外,与pDNA和mRNA相比,RNP的生产需求更多的人工成本。在蛋白质生产过程中,引入有毒污染物的可能性会增加,这为临床应用带来了安全风险。
电穿孔是将RNP送入细胞最有效的方法,并且在体外基因编辑和小鼠胚胎基因工程中具有成功的案例。然而,通过静脉注射含有RNP的LNP也已被证明对于将CRISPR组分靶向递送到肌肉、大脑、肺和肝脏是同样有效的方式。
基于RNP的CRISPR疗法当前已在临床应用中取得了成功——首-个基于CRISPR基因编辑的药物Casgevy获得FDA批准可用于治疗镰状细胞贫血。这种药物使用电穿孔将RNP形式的CRISPR组分体外递送至患者细胞,然后对这些编辑过的细胞进行筛选并回输给患者。